SOS MAINS
Syndrome du canal carpien
. Champagne-Ardenne .
Résumé :
Le syndrome du canal carpien est une pathologie fréquente. Il s’agit d’une compression du nerf médian lors de son passage dans le canal carpien. L’origine est variable, soit idiopathique (le plus souvent), soit secondaire à une pathologie ou un traumatisme. L’anatomie du nerf médian reste discutée en raison de nombreuses variations pouvant toucher le rameau thénarien mais aussi le nerf lui-même ou d’éventuels rameaux accessoires. Le diagnostic est essentiellement clinique basé sur le trépied paresthésies / réveils nocturnes / douleurs. La symptomatologie clinique peut parfois être polymorphe, entraînant des errances diagnostiques. L’électomyogramme est l’examen complémentaire essentiel, qui doit être demandé aussi bien pour conforter le diagnostic qu’à des fins médico-légales. Il existe cependant des faux négatifs et des faux positifs et c’est la clinique qui prime dans la décision thérapeutique. Les examens d’imagerie (IRM, échographie) sont utilisés accessoirement. Le traitement médical (orthèse de repos nocturne, infiltrations) peut être tenté en première intention sans qu’on ait pu évaluer son efficacité réelle. Le traitement chirurgical est partagé entre chirurgie à ciel ouvert et chirurgie endoscopique. La libération endoscopique du nerf médian au canal carpien permet d’obtenir des suites plus rapides qu’en chirurgie à ciel ouvert. Il est admis qu’à six mois de l’intervention, le résultat est identique pour les deux techniques. Les complications graves (section neurologique, artérielle, tendineuse) restent extrêmement rares avec la technique endoscopique et le taux global de complications est très faible (0.19%). La technique endoscopique nécessite un compagnonnage lors de la courbe d’apprentissage afin d’éviter des évènements indésirables. On estime que près de cent cinquante mille patients recourent au traitement chirurgical chaque année en France. Les récidives sont rares et doivent faire rechercher une libération incomplète. La libération endoscopique du nerf médian est aujourd’hui une technique bénéficiant de plus de trente ans de recul, parfaitement codifiée, et dont le taux de complications reste inférieur à celui des libérations à ciel ouvert.
INTRODUCTION
Le syndrome du canal carpien correspond à la manifestation clinique de la compression du nerf médian lors de son passage dans le canal carpien. La prévalence du canal carpien varie de 1 à 5% dans la population générale. La chirurgie de libération du nerf médian au canal carpien est récente, remontant au début des années 60 . Les techniques endoscopiques ont fait leur apparition au début des années 90 avec Agee et Chow. Le vieillissement de la population, le développement de la spécialisation chirurgicale et l’apparition des techniques endoscopiques ont probablement concouru à l‘envolée du nombre d’interventions. Si en 1995, on dénombrait 9 537 interventions de libération du nerf médian au canal carpien, ce chiffre était passé à 142 405 en 2005 et semble être resté stable depuis. Cette chirurgie, relevant à priori d’une compétence en chirurgie de la main est en réalité réalisée par des chirurgiens venant d’horizons divers et parfois très variés. L’apparente simplicité du geste (chirurgie à ciel ouvert) pousse un grand nombre de chirurgiens à s’intéresser à cette pathologie avec des résultats inégaux.
Le traitement du syndrome du canal carpien se répartit encore aujourd’hui entre traitement médical et chirurgical. Le traitement médical est proposé dans les formes débutantes et le traitement chirurgical dans les formes plus avancées. Le traitement chirurgical se répartit actuellement entre chirurgie à ciel ouvert (chirurgie classique ou mini-invasive) et chirurgie endoscopique.
Anatomie
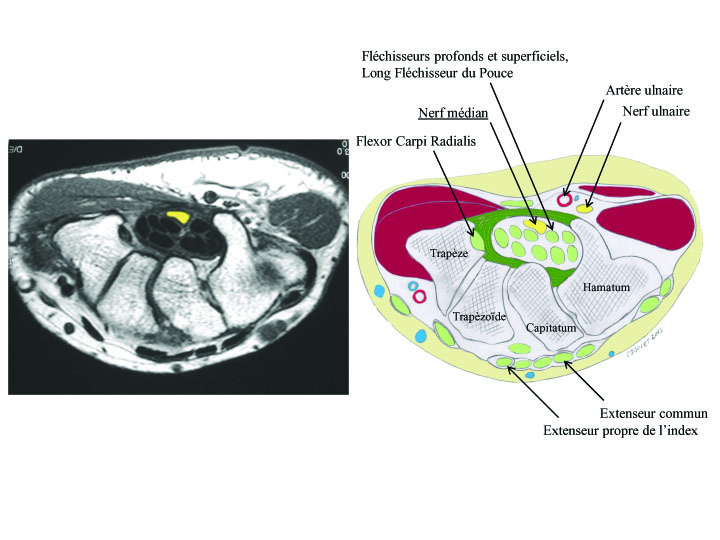
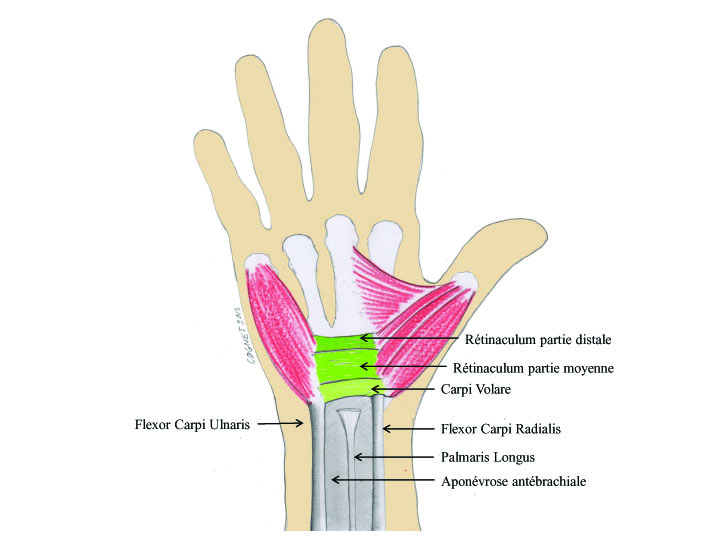
Le canal carpien est une structure anatomique qui se présente sous la forme d’un canal ostéo-fibreux inextensible situé à la partie proximale de la paume de la main. Il a la forme d’une gouttière constituée par les os du carpe, et fermée par un épais ligament : le rétinaculum des fléchisseurs (retinaculum flexorum). Le rétinaculum des fléchisseurs est lui-même subdivisé en trois parties. La partie proximale fait suite à l’aponévrose antébrachiale antérieure et correspond au carpi-volare. La partie moyenne, plus épaisse, couvre la partie la plus étroite du canal carpien. Vient ensuite la partie distale qui relie les éminences thénar et hypothenar. Pour Cobb et al, il existe deux zones de compression potentielles dans le canal carpien. La première correspond à la partie proximale, c’est-à-dire à la fin de l’aponévrose brachiale antérieure et au carpi volare. Il est assez fréquent, lors de chirurgie à ciel ouvert de retrouver un aspect en sablier du nerf médian dans cette zone proximale, témoignant de la compression. La seconde zone de compression serait d’après Cobb et al la zone la plus étroite correspondant à l’hamulus de l’hamatum. Cette notion est plus discutable et pour Chow et al, la forme et l’importance de l’hamulus de l’hamatum pourraient jouer un rôle prédisposant dans la compression du nerf médian. Le canal carpien s’étend du radius distal à la base du troisième métacarpien sur environ 3 à 4 cm. Le rétinaculum des fléchisseurs est tendu entre la base du scaphoide et le trapèze sur son versant radial et l’hamulus de l’hamatum et le pisiforme du coté ulnaire. Sur son versant radial, le Flexor Retinaculum se divise en feuillet profond et superficiel, laissant le passage au Flexor Carpi Radialis. Le canal carpien a une largeur de 20 mm au centre et de 25 mm en proximal et distal prenant la forme d’un sablier. A l’intérieur du canal carpien cheminent le nerf médian et 9 tendons : le Long Fléchisseur du Pouce, les 4 tendons Fléchisseurs Superficiels et les 4 tendons Fléchisseurs Profonds des doigts. Le Fléchisseur Radial du Carpe, le Fléchisseur Ulnaire du Carpe et le Palmaris Longus cheminent en dehors du canal carpien. Le nerf médian se situe au dessus du fléchisseur superficiel de l’index. Il se divise, après sa sortie du canal carpien en un rameau moteur (rameau thénarien innervant le faisceau superficiel du court fléchisseur, court abducteur et opposant) et en plusieurs rameaux sensitifs : les nerfs digitaux commun des premier, deuxième et troisième espace et le nerf collatéral radial du pouce. Il faut garder à l’esprit que le canal de Guyon se situe sur la face antérieure et ulnaire du canal carpien le recouvrant sur 30% de sa surface.
Ce qu’il faut retenir de l’anatomie du nerf médian et du canal carpien :
l’anatomie dite « classique » du nerf médian lors de son passage dans le canal carpien (situation radiale, en regard du fléchisseur superficiel de l’index, rameau thénarien extra-ligamentaire radial) correspond à un pourcentage de patients non établi de façon formelle dans la littérature. De la même façon, des variations anatomiques plus ou moins importantes existent non définies par la littérature (variation de 1 à 70% des cas). Il faut toutefois prêter une plus grande attention en cas muscles thénariens recouvrant le retinaculum car il existe alors une corrélation avec des variations anatomiques du rameau thénarien.
Physiopathologie
Le syndrome du canal carpien repose sur un conflit entre le contenant (canal carpien) et le contenu (nerf médian et tendons fléchisseurs). Le manque d’espace dans le canal carpien entraîne une compression du nerf médian, responsable du syndrome du canal carpien. La compression du nerf médian au canal carpien peut-être idiopathique (pas de cause retrouvée) ou secondaire.
Dans le canal carpien idiopathique, on retrouve souvent une ténosynovite aspécifique. Il s’agit là de la forme la plus fréquente. Plusieurs études ont démontré qu’il existait une diminution du volume du canal carpien comparé à des patients aymptomatiques ainsi qu’un déterminisme génétique : nous sommes prédisposés ou non (comme pour l’arthrose de hanche) à développer une compression du nerf médian au canal carpien. Lozano-Calderon et al, à partir d’une méta-analyse sur les causes du syndrome du canal carpien ont démontré que l’activité professionnelle n’avait pas été validée en tant qu’étiologie potentielle.
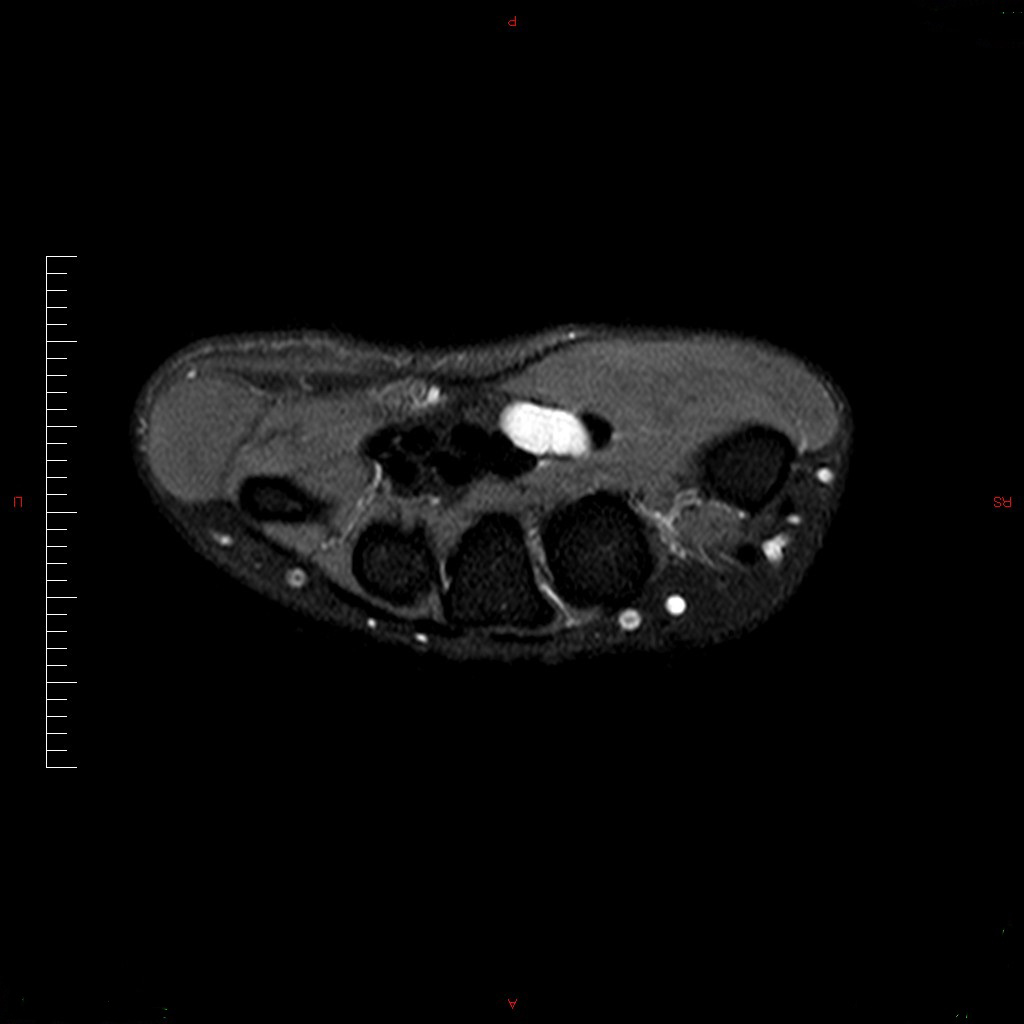
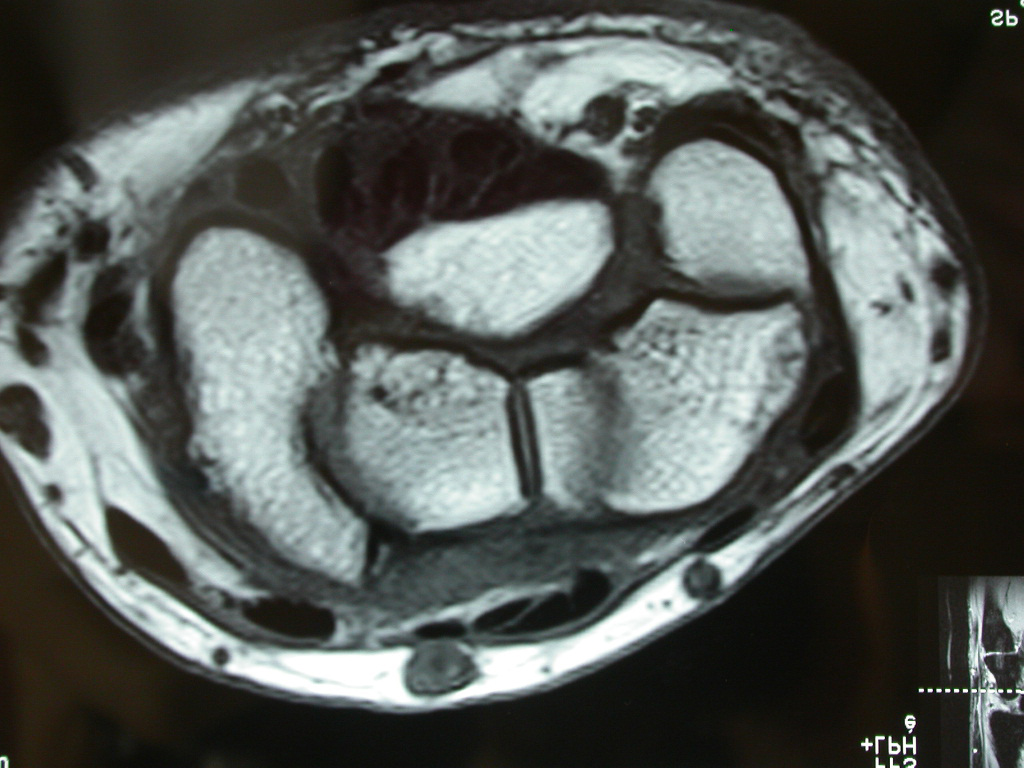
Le syndrome du canal carpien peut être secondaire à une multitude de pathologies médicales (diabète, polyarthrite rhumatoïde, amylose, arthrites microcristallines, acromégalie, obésité, mucopolysaccharidose, hypothyroïdie, sclérodermie, infection, etc.). La grossesse peut également aboutir à un syndrome du canal carpien, mais celui-ci est habituellement transitoire et disparaît en quelques semaines après l’accouchement. On peut retrouver des causes post-traumatiques amenant à un retrécissement du canal carpien comme une séquelle de fracture du radius distal ou une luxation rétro-lunaire du carpe passée inaperçue. Enfin, des processus expansifs (tumeurs, kystes, etc.) ou des anomalies anatomiques comme un palmaris profundis, un muscle lombrical hypertrophique, un muscle fléchisseur accessoire sont régulièrement rapportés.
Sur le cliché à gauche on retrouve un kyste (aspect arrondi, couleur blanche) alors que sur le cliché de droite, il y a un os en plus dans le canal carpien, séquelle d’une luxation ancienne du poignet.
Examen clinique
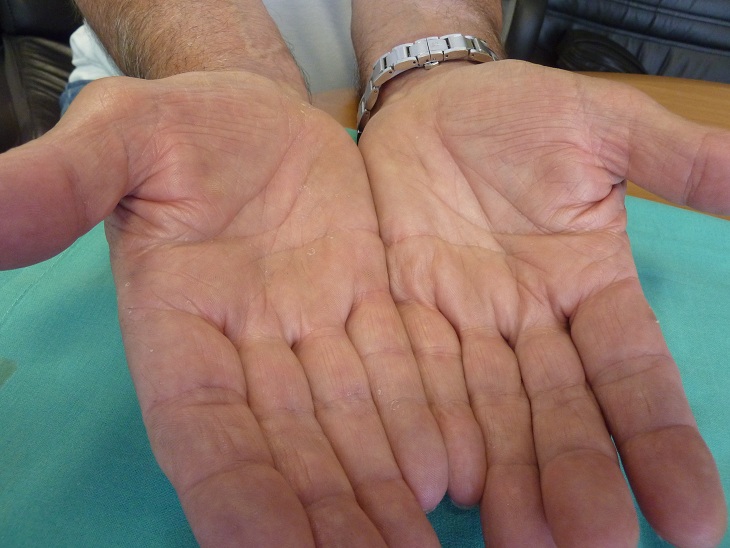
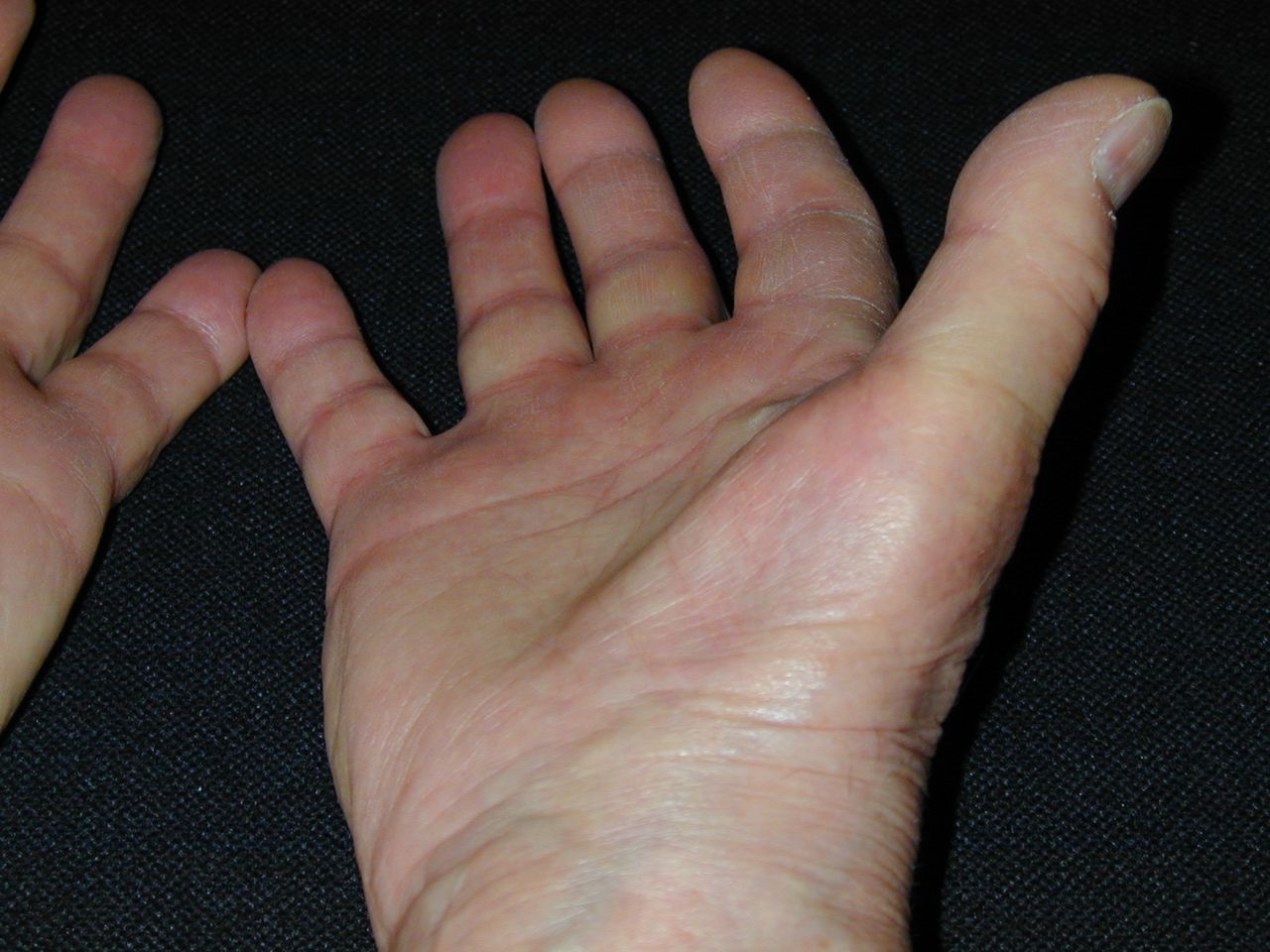
Le diagnostic clinique repose sur le trépied clinique paresthésies/réveils nocturnes/douleurs du membre supérieur. Les paresthésies peuvent être uniquement nocturnes, provoquant le réveil du patient, ou diurnes, intermittentes ou permanentes avec une expression clinique variable (gène retrouvée classiquement pour la conduite, la lecture et l’utilisation du téléphone). Les patients décrivent la nécessité de changer de position ou de secouer la main pour obtenir la disparition des paresthésies lorsque celles-ci sont intermittentes. L’évolution peut se faire vers une hypoesthésie puis une anesthésie du territoire médian (stade avancé). Les réveils peuvent survenir en fin de nuit ou tout au long de la nuit en plusieurs épisodes. Les douleurs peuvent être concentrées au niveau de la main ou du poignet (douleur sourde, plutôt en regard du canal carpien) ou s’étendre jusqu’à l’épaule ou au rachis cervical. Parfois même, la douleur est prééminente au niveau de l’épaule ou du cou ce qui peut entraîner un retard diagnostique. Le score de Katz et Stirrat, peu utilisé en France est un algorythme permettant d’évaluer la probabilité diagnostique de compression du nerf médian au canal carpien. La manœuvre de Phalen, souvent utilisée a une sensibilité de 60% et une spécificité de 80%. En règle générale, les antalgiques de niveau I et II sont inefficaces face à ces douleurs (ce qui est un bon argument diagnostique). Seuls des médicaments de type RIVOTRIL peuvent avoir une efficacité modérée. Une infiltration de stéroïdes dans le canal carpien est plus efficace et peut servir de test diagnostique et thérapeutique. Dans les formes vieillies, il existe une atrophie de l’éminence thénar et une paralysie de l’opposition du pouce.
Noter l’atrophie de l’éminence thénar dans le cadre d’une compression ancienne du nerf médian au canal carpien.
Cas particuliers du canal carpien chez, l’enfant, l’adolescent ou le jeune adulte
La survenue d’une compression du nerf médian chez un sujet jeune ou un enfant peut correspondre à un canal carpien constitutionnellement étroit idiopathique. Dans ce cas de figure, on recherchera des antécédents familiaux. Il faut aussi évoquer la possibilité d’un processus intra-canalaire surtout si la symptomatologie clinique est unilatérale et demander alors une IRM. Chez ces jeunes patients, enfants, adolescents et adultes jeunes, le tableau clinique peut être atypique, centré uniquement sur la douleur et retarder le diagnostic.
Examens complémentaires
Electromyogramme
L’électromyogramme (EMG) mesure les vitesses de conduction des fibres sensitives et motrices. C’est un examen désagréable pour le patient, plutôt long, et opérateur dépendant. Il existe différents types d’appareils, qui doivent être étalonnés et la comparaison de deux tracés réalisés sur deux appareils différents est souvent difficile.
La sensibilité de cet examen est de 86% et sa spécificité de 83% ce qui aboutit à des faux négatifs (patients avec une symptomatologie clinique typique mais un EMG négatif) et à des faux positifs (patients asymptomatiques mais avec un EMG positif). Les faux négatifs se voient surtout dans les formes débutantes ou peuvent être expliquées par le fait que l’EMG ne teste que les grosses fibres nerveuses.
Cet examen permet de mesurer l’amplitude des réponses motrices et sensitives et éventuellement leur diminution (perte axonale, qui est un signe de gravité). La compression nerveuse se traduit par un allongement des latences distales et par un ralentissement des vitesses de conduction motrice et sensitives. La vitesse de conduction motrice est moins fiable que la vitesse de traversée sensitive. Dans les cas difficiles on peut utiliser des techniques de comparaison des latences entre cubital et médian après stimulation sur l’annulaire. La deuxième partie de l’EMG étudie les muscles et permet de rechercher des signes de gravité (tracé appauvri et accéléré dans le muscle court abducteur du pouce).
L’électromyogramme n’est pas obligatoire mais est fortement recommandé y compris dans le guide des bonnes pratiques publié en 2013 par l’HAS. De plus, un EMG pré-opératoire servira de référentiel en cas d’évolution défavorable post-opératoire. Il s’agit d’un examen opérateur dépendant d’où la nécessité d’avoir un correspondant (neurologue, rhumatologue, rééducateur fonctionnel) rompu à ce type de pratique. Cependant, cet examen n’a pas de valeur prédictive en terme de résultat et il est admis que sa négativité ne peut exclure l’existence d’une compression avérée du nerf médian au canal carpien.
Imagerie
- Radiographies : n’ont pas d’intérêt en dehors d’antécédents traumatiques ou d’une déformation du poignet
- Echographie : examen indolore, court avec une sensibilité de 70 à 94% et une spécificité de 57 à 98% pour le diagnostic d’une compression du nerf médian au canal carpien. Cet examen peut montrer une synovite des fléchisseurs, un processus intra-canalaire ou un œdème du nerf et peut être demandé en cas de présentation atypique (patient jeune, un seul coté atteint) ou en cas de dissonance entre l’EMG et la symptomatologie clinique. A l’avantage d’être peu onéreux. A l’inconvénient d’être opérateur dépendant, avec des clichés non interprétables. Malgré son innocuité, son faible coût et les informations qu’il apporte en terme d’exploration du canal carpien, cet examen ne peut, aujourd’hui, remplacer l’EMG.
- IRM : demandée rarement en première intention, utilisée plutôt en seconde intention après l’échographie pour préciser l’exploration du canal carpien.
TRAITEMENT
Traitement médical
Recommandé par l’HAS en première intention dans les formes dites « peu sévères », sans atrophie musculaire ou signe de perte axonale à l’EMG. Rappelons toutefois que l’évolution naturelle de la compression du nerf médian au canal carpien est mal connue et qu’il n’existe pas, aujourd’hui, d’études de cohorte suivant des patients non traités ou traités médicalement. Parmi les traitements médicaux proposés pour la prise en charge médicale du canal carpien, on relève :
- Le port d’une orthèse de repos nocturne : proposé de façon classique car peu onéreux et sans danger, n’a jamais fait la preuve de son efficacité comme en témoigne la dernière méta-analyse en provenance de la Cochrane Database. Cet article reprenant 19 études randomisées chez 1190 patients ne retrouve pas de supériorité d’une attelle par rapport à une autre ou du port d’une attelle par rapport à l’absence de traitement.
- L’injection de corticoïdes dans le canal carpien. Ces injections doivent être limitées au nombre de 3. L’effet est retardé de quelques jours à quelques semaines et l’efficacité est variable dans le temps et en fonction des patients. Pour Weiss et al, ce traitement est surtout efficace chez les patients âgés de moins de 40 ans. Cette injection comporte un risque de léser le nerf de façon transitoire ou définitive. Dubert et al ont proposé de réaliser l’infiltration en passant au travers du Flexor Carpi Radialis, c’est-à-dire à distance du nerf médian, celui-ci se situant sous le palmaris longus.
- D’autres traitements comme l’adjonction de Béta-carotène, de vitamine B6, la pratique du yoga, l’acuponcture, l’utilisation du laser, la magnétothérapie n’ont pas fait la preuve de leur efficacité.
Traitement chirurgical
Quand faut-il poser l’indication opératoire ?
Cette question trouve sa réponse dans la pratique clinique régulière, corroborée par les données de la littérature. Comme souvent, c’est la clinique qui prime par rapport aux examens complémentaires. Nous avons vu précédemment que l’électromyogramme comportait des faux négatifs et des faux positifs et qu’il ne pouvait s’agir en aucun cas de l’examen de « l’absolue certitude ». L’indication opératoire doit être posée avant tout sur la gêne ressentie par le patient. L’échec du traitement médical renvoie rapidement au traitement chirurgical. Des facteurs « extérieurs » peuvent également rentrer en ligne de compte dans le choix décisionnel du patient comme une expérience rapportée de cette intervention par un proche (positive ou négative), le fait de pouvoir compter sur une aide pour la convalescence, ou le niveau d’indemnisation pendant la période d’arrêt post-opératoire.
Traitement à ciel ouvert
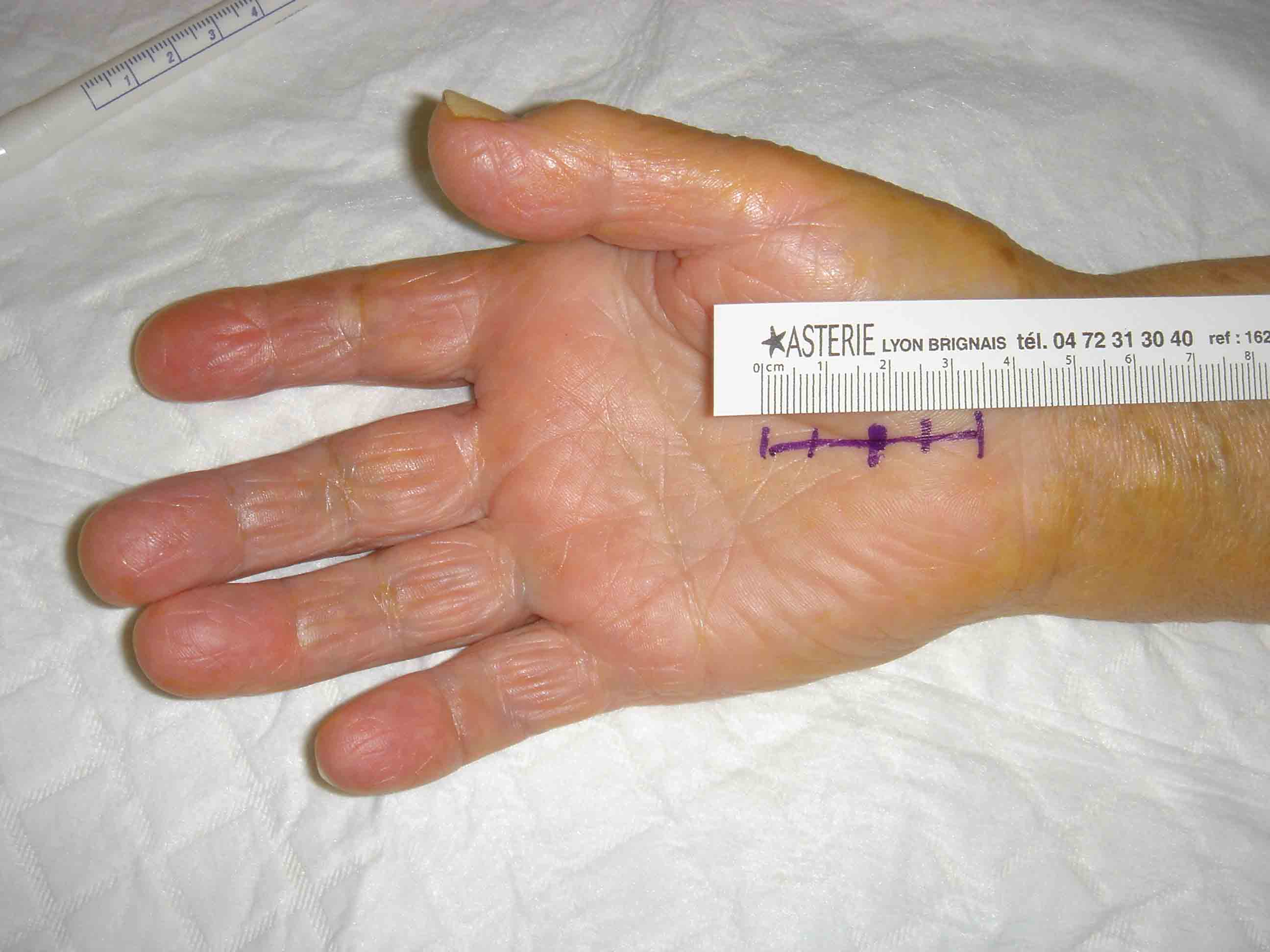
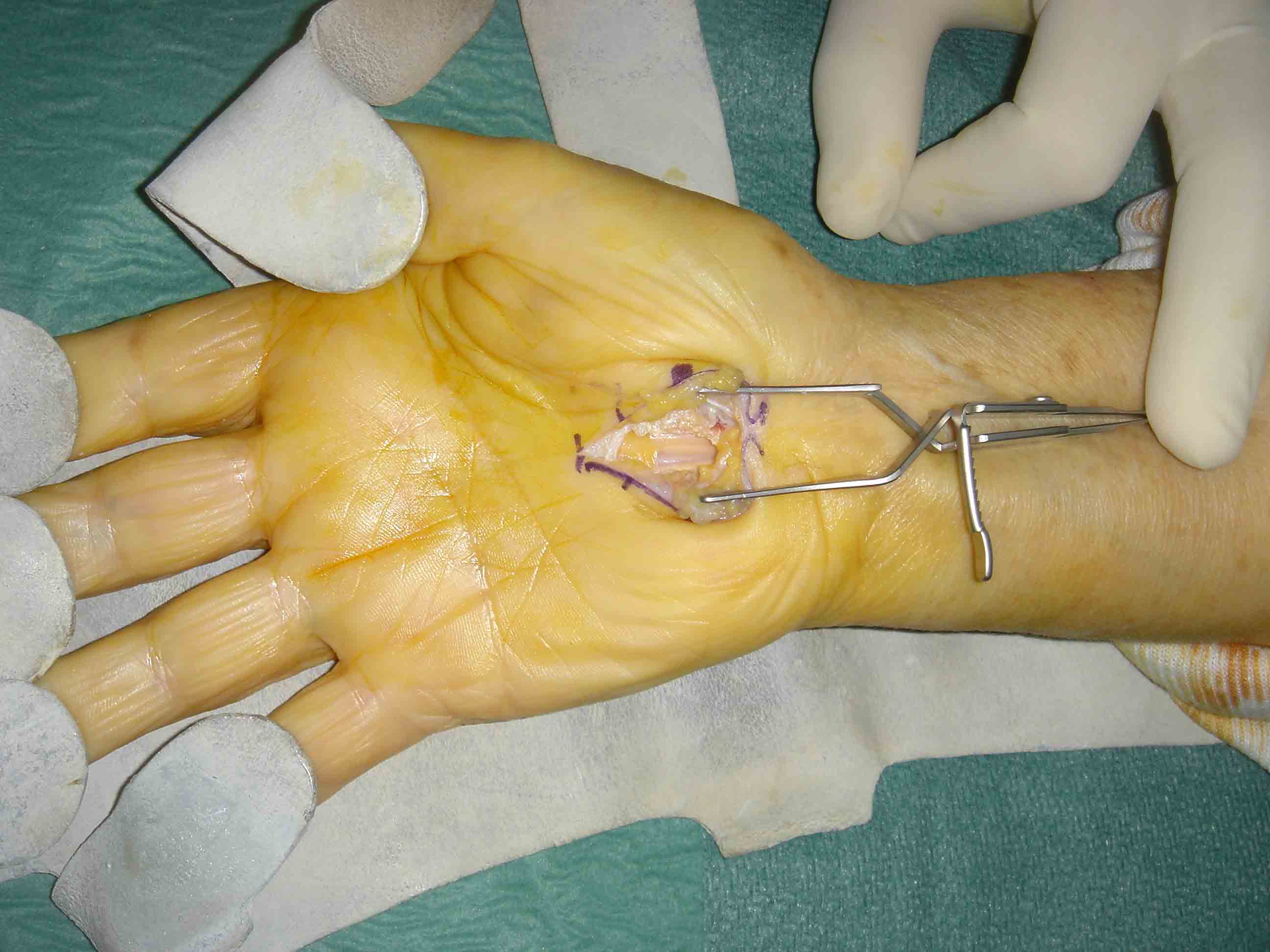
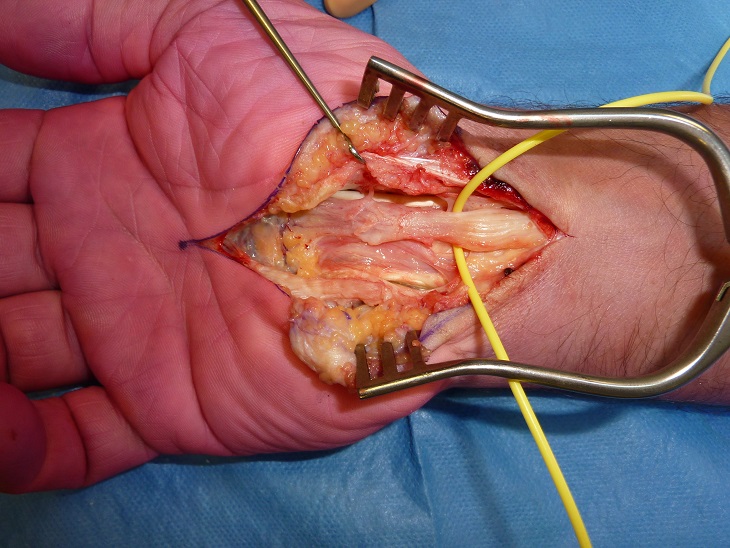
Le patient est installé en décubitus dorsal, le bras en abduction sur une table à bras. L’incision est plus ou moins longue étant considéré qu’en deçà de 3 cm, on parle de technique mini-invasive. L’axe de l’incision est celui du troisième espace interdigital. Elle peut être débutée en amont du pli de flexion du poignet au niveau du carpi-volare et s’étendre jusqu’en aval de la partie distale du rétinaculum. Le principe de cette voie est de voir le nerf, d’inspecter le canal carpien et de rechercher le rameau thénarien. Il n’est donc pas logique d’être économe sur la longueur de l’incision. L’inspection du canal carpien permet de rechercher des processus expansifs intra-canalaires (tumeur, kyste, muscle surnuméraire, etc.). La synovectomie des tendons fléchisseurs n’est pas nécessaire sauf dans certaines pathologies (pathologies rhumatismales, dialyse, etc.). La chirurgie à ciel ouvert peut également être utilisée lors d’une révision chirurgicale. L’incision de révision est en général plus longue que celle de la première intervention car il faut aborder le nerf médian en zone saine.
Traitement à ciel ouvert du canal carpien ; à droite, reprise d’un patient précédemment opéré nécessitant une incision plus importante.
Traitement par technique mini-invasive
La technique mini-invasive est apparue dans les suites du traitement endoscopique. Il s’agissait de rester « concurrentiel » en chirurgie ouverte face à des incisions réduites réalisées lors de la libération endoscopique. L’installation se fait en décubitus dorsal avec un garrot pneumatique à la racine du membre supérieur. L’incision peut se faire en proximal ou en distal suivant les habitudes de l’opérateur et reproduit les incisions de la technique endoscopique qu’il s’agisse de la technique à une voie ou de la technique à 2 voies. Dans la technique décrite par Benquet, l’opérateur utilise une sonde cannelée dont l’extrémité a été au préalable recourbée et un bistouri froid monté avec une lame de bistouri de 11. L’abord se fait au pli de flexion du poignet, dans l’axe du troisième espace. Le carpi volare est incisé et la sonde cannelée introduite dans le canal carpien. L’extrémité recourbée permet de repérer et de crocheter l’extrémité distale du retinaculum tout en protègeant l’arcade palmaire. La lame de 11 est ensuite poussée dans la sonde cannelée jusqu’à buter sur son extrémité recourbée. Une fois la sonde retirée, il est possible de vérifier la section du retinaculum en se plaçant dans l’axe de l’incison et en réalisant une traction sur les écarteurs. Des systèmes à usage unique (couteux) sont proposés par les industriels utilisant une lame en U associée à une lumière froide. Le retinaculum est positionné au centre de la lame puis le couteau est poussé jusqu’à obtenir la section complète du retinaculum. Cette technique consistant à couper « à l’aveugle » le retinaculum ne paraît pas dénuée de risques (variations anatomiques du nerf médian et de ses branches). Si certaines séries rapportées dans la littérature ne font pas état de complications spécifiques, d’autres rapportent des cas de section complète du nerf médian.
Image de gauche : technique mini-invasivé décrite par le Dr Benquet. A droite couteau lumineux utilisé en technique mini-invsive.
Traitement endoscopique
La technique de libération du nerf médian au canal carpien a été rapportée dans la littérature internationale par Okutsu en 1989 (81), 2 ans après une première publication en Japonais. Initiée au début des années 90 par Chow (21) et Agee (2) elle est maintenant utilisée en pratique courante même si ce n’est pas forcément le traitement le plus usité. Une étude récente de l’ASSH (63) portant sur l’ensemble du territoire américain retrouvait seulement 36% de chirurgien utilisant couramment la libération endoscopique du nerf médian au canal carpien et 52% ne l’utilisant jamais. Plusieurs facteurs rentrent en considération dans le choix d’une technique dite conventionnelle (à ciel ouvert) comparée à une technique endoscopique. Les séries monocentriques évaluant la technique endoscopique ont évolué au fil du temps avec une diminution du taux de complications (2, 3, 4, 8, 33, 80, 83) Les séries de la littérature, comparant les deux techniques ont abouti au fil du temps aux mêmes conclusions (1, 2, 59, 73, 104, 111). Libération à ciel ouvert et libération endoscopique du nerf médian au canal carpien aboutissent à 6 mois de l’intervention au même résultat clinique, avec un taux de complications proche. Les suites immédiates de la technique endoscopique sont plus rapides (3, 59) avec une durée d’arrêt de travail inférieure (97) à conditions que les patients ne bénéficient pas d’une protection sociale trop importante (28). Le choix du traitement arthroscopique nécessite un investissement important avec l’achat de plusieurs ancillaire dédiés, d’une colonne vidéo (pouvant être utilisée également pour la pratique de l’arthroscopie). De plus, les techniques les plus en vogue utilisent des couteaux endoscopiques à usage unique ce qui renchérit le coût. A l’opposé, la chirurgie dite conventionnelle (à ciel ouvert) n’utilise aucun matériel spécifique ce qui n’entraîne pas de surcoût. Cependant, Leger et Bustamente (62) ont montré que le coût global en France de la technique endoscopique était en fin de compte moins élevé que le coût de la chirurgie ouverte. Tenant compte du coût du matériel, et de la durée des soins (comprenant la rééducation), cette différence s’exerçait sur la durée de l’arrêt de travail, la technique endoscopique amenant à une reprise d’activité plus rapide.
Matériel
La pratique de l’endoscopie pour la libération du nerf médian nécessite l’accès à une colonne d’arthroscopie, si possible Haute Définition, avec au mieux un système d’enregistrement. Il existe des caméras autoclavables (couteuses) et des caméras plus classiques, isolées par une housse de protection. Il faut avoir à sa disposition plusieurs ancillaires compte-tenu du fait qu’il s’agit d’une intervention fréquente et qu’il est habituel pour un opérateur rompu à cette chirurgie d’opérer plusieurs canaux carpiens à la suite au cours d’une même vacation opératoire. Il peut s’agir d’un investissement important en fonction du matériel utilisé. L’instrumentation chirurgicale nécessaire à la pratique du canal carpien endoscopique est limitée (figure 11). En plus du matériel spécifique lié à l’ancillaire utilisé, un bistouri supportant une lame de 15, des ciseaux de Metzenbaum, un crochet de Gillis, une pince d’Addson sont nécessaires ainsi qu’éventuellement un porte-aiguille et des ciseaux de Mayo. Il est ainsi possible de se constituer un « kit canal carpien endoscopique » qui peut être mis dans la même boite que l’ancillaire dédié. Un produit anti-bué est régulièrement utilisé pour l’optique.
Technique à une voie utilisant le matériel d’AGEE
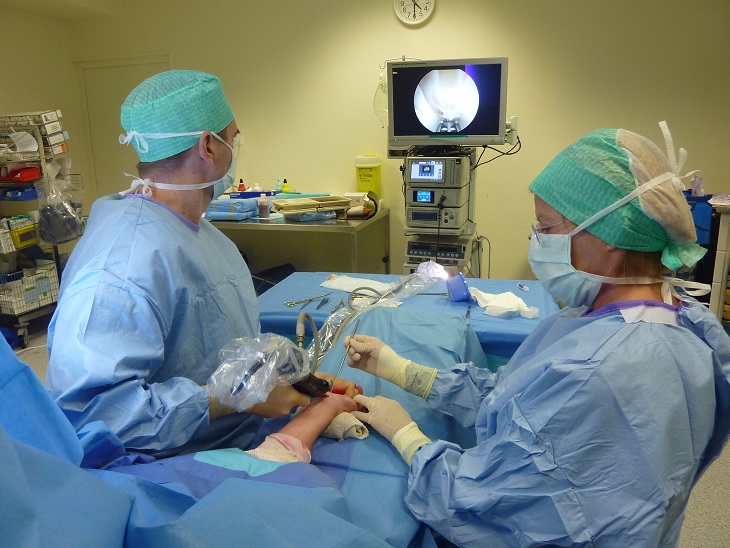
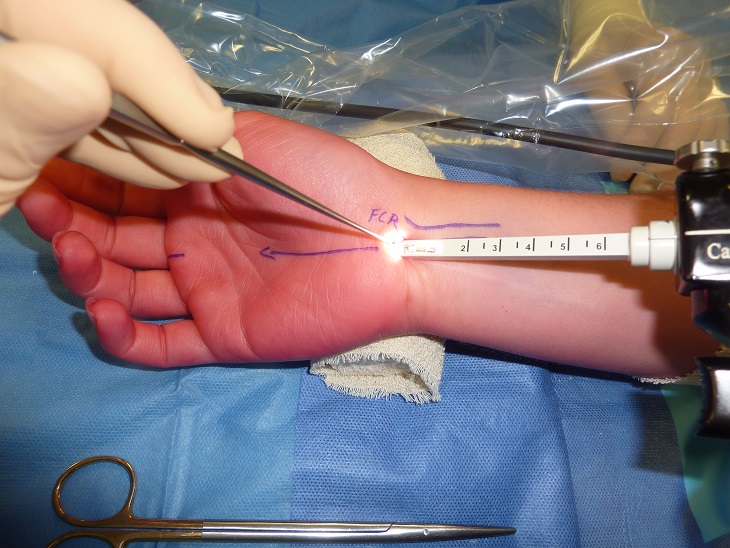
Le patient est installé en décubitus dorsal, avec une table à bras, épaule à 90°, paume vers le ciel. L’anesthésie peut être locale pure soit en réalisant un bloc du nerf médian, soit au contraire en réalisant une anesthésie des tissus mous. Une anesthésie loco-régionale permet d’utiliser un garrot le temps nécessaire à l’intervention, qui peut être plus ou moins rapide en fonction du niveau d’expérience de l’opérateur. Il faut également tenir compte de la nécessité éventuelle d’une conversion à ciel ouvert. Cependant, il est tout à fait possible de réaliser cette intervention sous anesthésie locale pure. On doit s’assurer lors de la consultation pré-opératoire qu’il n’existe pas de raideur de l’épaule empêchant la position en rotation externe supination nécessaire à la bonne réalisation de l’intervention. Le badigeon réalisé à la Bétadine remonte jusqu’au garrot situé au niveau du bras. L’opérateur se place dans l’aisselle du patient qu’il soit droitier ou gaucher, et qu’il s’agisse d’un canal carpien droit ou d’un canal carpien gauche. Ceci implique pour l’opérateur d’être ambidextre. Cette installation impliquant d’opérer du coté dominant ou non dominant se justifie par une tendance à la pronation automatique de l’avant bras lors du geste chirurgical. En opérant un canal carpien droit de la main droite et un canal carpien gauche de la main gauche, le mouvement automatique de pronation entraîne une dérive potentielle du couteau arthroscopique plutôt en situation ulnaire, ce qui représente un moindre danger de lésion du nerf médian. A l’inverse, un opérateur droitier, opérant un canal carpien gauche (opérateur à la tête du patient) devra positionner le bras (gauche) du patient en supination forcée, alors que le mouvement naturel de l’opérateur a tendance à enrouler l’avant bras en pronation ; le risque de lésion du nerf médian est, dans ce cas, plus important. La colonne vidéo est positionnée au bout de la table, dans un angle de 30° à partir du bras du patient en direction de sa tête.
Matériel d’Agee utilisé majoritairement en France pour la libération endoscopique du nerf médian au canal carpien.
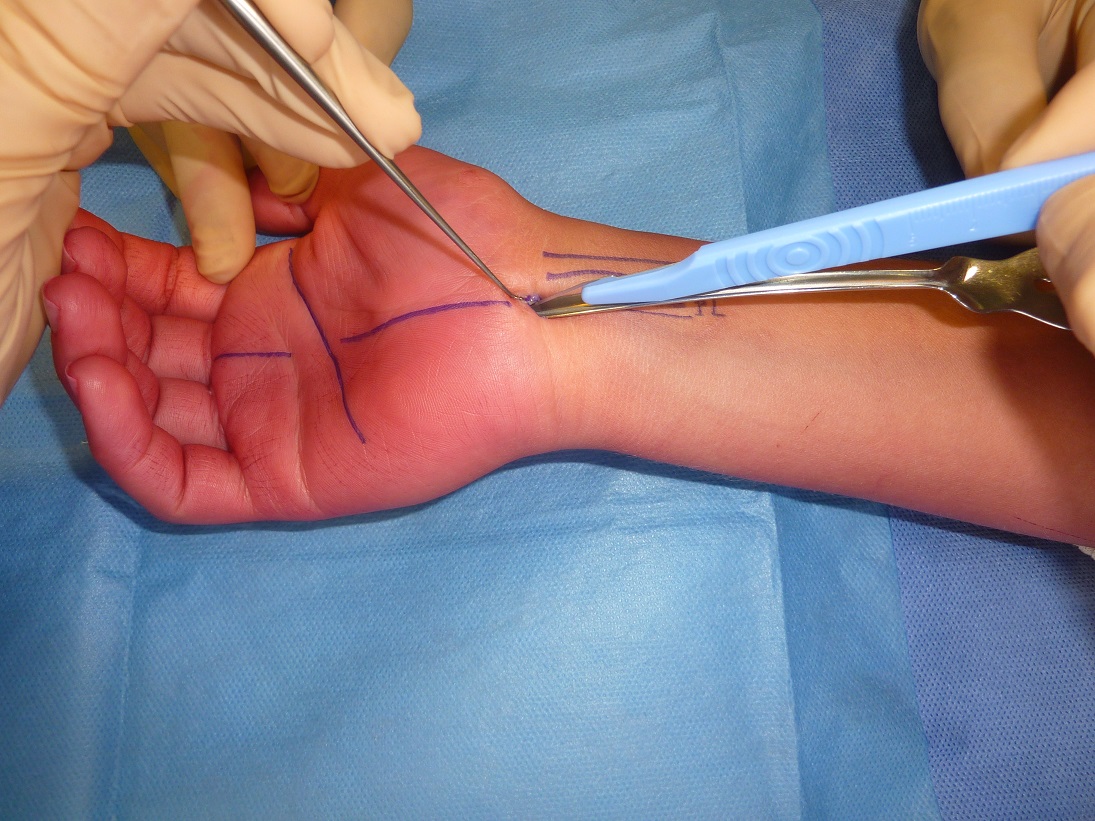
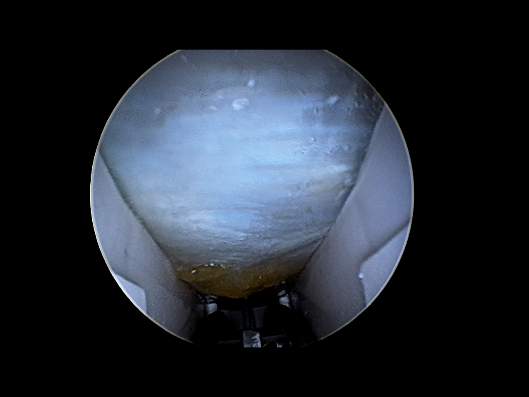
L’abord chirurgical se fait en utilisant un bistouri froid avec une lame de 15. La peau est incisée à minima pour éviter de léser le réseau veineux sous-cutané. Des ciseaux de Metzenbaum sont utilisés pour disséquer les tissus mous jusqu’à la face superficielle du retinaculum. A ce stade, il faut prendre le temps de bien visualiser la face superficielle du carpi volare qui est reconnaissable à son aspect blanc nacré et crénelé. Le bistouri froid est à nouveau utilisé pour inciser le carpi volare, pas à pas, sur 10 mm, suivant une direction perpendiculaire à l’axe de l’avant bras. Un crochet de Gillis est positionné sur la partie distale du rétinaculum, ce qui permet de le tracter vers le haut. Le nerf médian peut alors être visualisé. Une rugine est introduite à la face profonde du retinaculum et poussée au contact de celui-ci afin de le libérer de la synoviale.
L’introduction de l’optique dans le canal carpien doit pouvoir se faire sans « forcer ». La libération peut être considérée comme suffisante quand l’écart produit par la section du retinaculum permet l’ascension du couteau arthroscopique entre les deux parties du ligament sectionné . En tournant l’optique alternativement vers la droite ou la gauche, on peut voir les tranches de section du ligament ainsi que le nerf médian (et s’assurer ainsi de son intégrité). Une fois la section du rétinaculum réalisée, l’optique peut être introduit à plusieurs reprises dans le canal carpien jusque dans la paume de la main sans rencontrer de résistance.
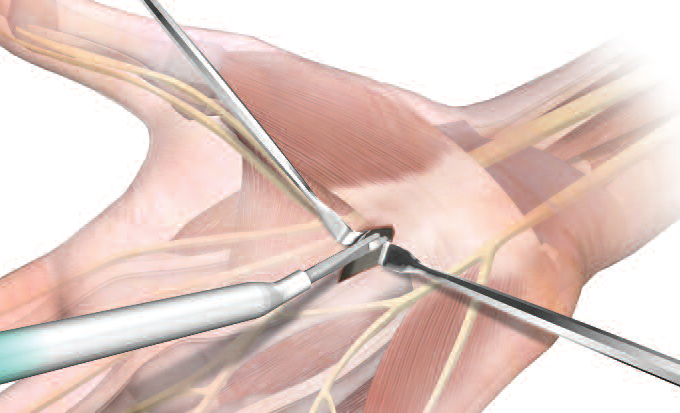
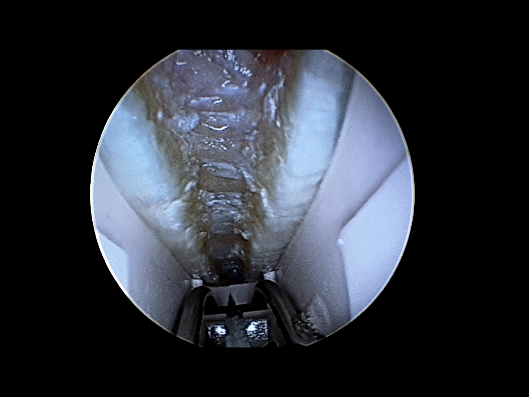
Après introduction de l’optique dans le canal carpien, le retinaculum est parfaitement visualisé et sectionné à l’aide de la lame rétractable.
La fermeture peut-être réalisée au choix par un point de suture ou par des stéristrips. Un pansement sec léger suffit habituellement. Il vaut mieux lâcher le garrot lors du pansement pour s’assurer de l’absence de saignement intempestif, en règle générale veineux, qui peut nécessiter un pansement compressif transitoire. L’immobilisation post-opératoire, longtemps utilisée, n’a jamais démontré son intérêt et n’est pas nécessaire, voire nocive car favorise les adhérences du nerf médian dans le canal carpien en faisant disparaître son espace de glissement. Les patients sont encouragés à se servir de leur main le plus rapidement possible en limitant leurs activités en fonction de la gêne ressentie. L’arrêt de travail varie de 15 jours à un mois.
Suites opératoires / Résultats
Les réveils nocturnes et les douleurs du membre supérieur disparaissent rapidement après l’intervention, parfois le soir même suivant l’acte chirurgical. Les paresthésies disparaissent sur une période variable liée à l’importance de la compression du nerf médian et à la durée de la compression ayant précédé l’intervention. Il persiste habituellement une douleur du talon de la main et une diminution de 50% de la force de serrage pendant une durée de 2 à 4 mois. Il faut prendre le temps, lors de la consultation pré-opératoire, d’expliquer au patient cette notion de « résultat en 2 temps » et lui remettre un document écrit, lui rappelant le déroulement des suites opératoires ainsi que les contre-indications post-opératoires.
La consultation de contrôle post-opératoire est réalisée entre la première et la troisième semaine. C’est le moment où les patients reprennent leur activité (personnelle ou professionnelle) qui s’accompagne habituellement d’une phase douloureuse sur les efforts ou l’appui du talon de la main. Lors de cette consultation, on doit s’assurer de la disparition des acroparesthésies nocturnes, des douleurs du membre supérieur et prendre le temps de réexpliquer au patient que la récupération complète est attendue vers la fin du quatrième mois.
La rééducation n’est pas justifiée après chirurgie du canal carpien, à quelques exceptions près.
Complications
Sont heureusement rares comme en témoignent les séries de la littérature. Ces complications sont plutôt rencontrées lors de la courbe d’apprentissage. Le taux global de complications est estimé aujourd’hui à 0.49% pour la chirurgie ouverte et 0.19% pour la chirurgie endoscopique, sachant que le taux de complications en chirurgie ouverte est certainement sous-estimé.
Récidive / absence d’amélioration post-opératoire.
L’absence d’amélioration ou la récidive précoce posent un problème à la fois diagnostique et thérapeutique. Stutz et al dans une série rétrospective de 200 patients opérés à deux reprises d’une libération du nerf médian au canal carpien ont retrouvé 54% de libération incomplète, 23% de cicatrices hypertrophiques, 9% de fibrose périneurale, 6% de lésion neurologique, 2% de tumeurs bénignes et 7% de cas inexpliqués. Cobb et al ont toutefois démontré qu’une section incomplète du rétinaculum des fléchisseurs n’était pas corrélée statistiquement au résultat clinique. Beck et al ont proposé de réaliser une infiltration de stéroides avant reprise chirurgicale. Ils ont démontré que cette infiltration avait une grande sensibilité et une importante valeur prédictive (87%) en terme de succès chirurgical secondaire. Il faut alors envisager une reprise chirurgicale à ciel ouvert car une section incomplète du rétinaculum, venant comprimer un des nerfs de division peut parfois simuler une atteinte neurologique (anesthésie en portefeuille). L’inspection du nerf est nécessaire pour lever tout doute. Cette reprise peut-être envisagée vers le troisième mois car, dan un canal carpien particulièrement étroit, l’introduction de la canule endoscopique peut entrainer une neurapraxie qui disparaîtra spontanément en quelques semaines. L’IRM a été proposée pour rechercher des sections incomplètes mais la définition courante des IRM disponibles actuellement (fenêtres de 3 à 4 mm) ne permet pas de diagnostic de certitude. D’autre part, l’aspect IRM post canal carpien endoscopique à 3 mois ne permet pas de retrouver la zone de section, contrairement à l’aspect IRM post canal carpien à ciel ouvert. L’IRM peut par contre montrer un processus expansif intra-canalaire (muscle surnuméraire, tumeur, synovite…). L’électromyogramme peut également être demandé mais là encore, quelque soit le résultat obtenu, il ne s’agit pas d’un diagnostic de certitude. Zyluc et Szlosser dans une étude récente, ont montré qu’il n’y avait pas de corrélation entre la symptomatologie clinique et l’électromyogramme concernant le résultat post-opératoire de la libération du nerf médian au canal carpien.
En résumé, face à la persistance de la symptomatologie ou à une récidive précoce, il n’existe pas d’examen permettant de poser avec certitude de diagnostic. Le seul intérêt de l’IRM est de rechercher une cause intra-canalaire de compression ou une section tronculaire, sans pouvoir donner d’information sur la qualité de la section du retinaculum dans le cadre d’une prise en charge endoscopique. L’electromyogramme est utile en terme de comparaison par rapport à l’examen pré-opératoire et pour l’évolution mais ne peut donner de diagnostic de certitude. Ces deux examens ont toutefois leur importance dans un cadre médico-légal. La chirurgie de reprise, en l’absence d’amélioration est en général nécessaire, dans un délai variant en fonction de la symptomatologie clinique, sachant que dans plus de 50% des cas, il s’agit d’une libération incomplète.
Reprise du travail
La durée moyenne de l’arrêt de travail après chirurgie du canal carpien est de 2 mois en France. Certains facteurs comme l’obésité, une chirurgie bilatérale, une pathologie associée du membre supérieur, la reconnaissance en maladie professionnelle, un arrêt de travail pré-opératoire un terrain dépressif, ou le degré de satisfaction des patients influencent la durée de l’arrêt de travail. Cowan et al dans une étude plus ciblée (technique mini-invasive) mais sur un échantillon de plus petite taille (65 patients) retrouve une durée moyenne d’arrêt de travail de 19 jours. A noter qu’aucun patient de cette série n’était pris en charge financièrement au titre de sa maladie. Le rapport entre le niveau de protection sociale et la durée de l’arrêt de travail a été étudié et a aboutit à la conclusion, dans certaines études, que l’arrêt est d’autant plus long que les processus de compensation financière mis en place sont importants. D’autres études n’ont pu mettre en évidence ce lien de causalité. Hansen a montré que, lorsque les patients bénéficient tous du même niveau de protection sociale, comme c’est le cas au Danemark où le patient perçoit un salaire plein pendant son arrêt, la durée moyenne de l’arrêt post-opératoire n’est plus que de 21 jours.
Le choix de la technique opératoire (endoscopique, mini-invasive, classique) rentre en ligne de compte mais son effet est apprécié diversement en fonction des séries publiées. Pour certains, la libération endoscopique permet un retour au travail plus rapide que la technique mini-invasive ou que la technique classique à ciel ouvert. Gerritsen et al, dans une méta-analyse publiée en 2001 confirmaient cette supériorité de la technique endoscopique. Thoma et al, dans une méta-analyse publiée en 2004 ne retrouvent pas de différence en terme de durée d’arrêt de travail entre les 3 techniques.
EVOLUTION
De nouvelles techniques ont vu récemment le jour. C’est le cas de la libération du nerf médian au canal carpien sous échographie. Décrite initialement en 1997 par Nakamichi et Tachibana , ceux-ci utilisaient une pince basket introduite par une vois d’abord palmaire dans un tube métallique fenêtré pour sectionner le rétinaculum. En comparant un groupe chirurgie ouverte versus chirurgie sous contrôle échographique, les auteurs notaient une récupération plus rapide du groupe échographie (en rapport avec la taille de la voie d’abord) et une absence de complications. Toutefois, la résolution limitée de l’échographe représentait pour eux un problème pour les groupes I et III de la classification de Lanz. Depuis 2011, d’autres séries ont été publiées rapportant soit des études de faisabilité, soit des études cliniques. Il n’existe pas de recul suffisant pour juger de l’efficacité et de l’innocuité de ces techniques actuellement. Il est toutefois probable que celles-ci vont se développer en parallèle de l’imagerie en gardant à l’esprit les problèmes inhérents aux variations anatomiques.
CONCLUSION
La libération endoscopique du nerf médian est une technique fiable, reproductible dont le taux de complications n’est pas supérieur à la chirurgie à ciel ouvert. Sa pratique nécessite un encadrement lors de la courbe d’apprentissage car c’est pendant cette courbe d’apprentissage que se produisent les évènements indésirables graves. Le résultat dépend de l’entrainement de l’opérateur mais également de l’indication opératoire (choix du patient). Il s’agit d’une technique relativement couteuse mais dont le surcoût peut être contrebalancé par une reprise du travail plus précoce. Les suites sont habituellement simples mais dépendent également de facteurs extérieurs comme le profil psychologique du patient, son âge, la protection sociale dont il bénéficie et son intégration dans la société.

Nous joindre
SOS Mains
1 rue Jules Méline,
51430 Bezannes
Pour les urgences, contactez le :
03 26 05 55 54